Newsletter
Impfen – eine altbewährte Methode zur Prävention von Infektionskrankheiten
Schutzimpfungen konnten bereits Millionen von Menschenleben retten., Bild: Pixabay, CCO
Im Laufe der Geschichte konnten durch Schutzimpfungen Millionen von Menschenleben gerettet werden. Trotzdem wird dieses Thema immer wieder kontrovers diskutiert. Dieser Artikel erläutert die geschichtlichen Hintergründe des Impfens, die dafür wichtigen Komponenten des Immunsystems, die biologischen Abläufe im Körper sowie die verschiedenen Arten von Impfstoffen, die heute zur Verfügung stehen. Seit dem Ausbruch der Corona-Pandemie ist dieses Thema aktueller denn je.
Von der Variolation zur heutigen Immunisierung
Impfungen zählen zu den größten Errungenschaften der Präventivmedizin. Mit der Ausnahme von sauberem Trinkwasser bewahrte im Lauf der letzten 200 Jahre keine andere Gesundheitsmaßnahme so viele Menschen vor dem Tod wie diese [1].
Der Mensch schützte sich bereits im 14. Jahrhundert nachweislich durch Quarantäne vor ansteckenden Krankheiten und Seuchen, war diesen jedoch lange Zeit relativ schutzlos ausgeliefert. Auch der Ursprung von Krankheiten war lange unbekannt. Erst als die Pocken Ende des 18. Jahrhunderts in Europa wüteten und hunderttausende Tote forderten, startete die Erfolgsgeschichte der Schutzimpfung. Pockenviren riefen schwere Erkrankungen mit hohem Fieber, Entzündungen und eitrigen Pusteln hervor, und rund ein Drittel der Erkrankten starb daran. Bekanntes Beispiel für Opfer der Pocken ist die Familie von Maria Theresia: Die Regentin verlor drei ihrer Kinder an diese Krankheit. In der zweiten Hälfte des 18. Jahrhunderts schaffte es dann die so genannte Variolation (Variolae = Pocken) – eine sehr alte Methode zur Immunisierung, die ursprünglich aus Indien stammt – nach Europa. Dafür wurde das Pustelsekret von Erkrankten auf die aufgeritzte Haut aufgetragen. Diese Methode war jedoch sehr riskant und unbeliebt. Der englische Arzt Edward Jenner änderte diese Art der Immunisierung leicht ab: Er beobachtete, dass Personen, die sich mit mild verlaufenden Kuhpocken infizierten, von den echten Pocken verschont blieben. In seinem berühmten Experiment im Jahr 1796 übertrug Jenner deshalb das Sekret einer Kuhpockenblase einer Stallmagd über einen Schnitt im Oberarm auf einen Jungen, der daraufhin leicht erkrankte. Einige Wochen später infizierte er den Jungen mit den echten Pocken, und der Junge blieb gesund. Dieses Experiment – das aus heutiger Sicht höchst unethisch ist – galt damals als großer Durchbruch und stellt die Geburtsstunde der ersten Schutzimpfung dar. Ein Bekannter Jenners, Richard Dunning, prägte um die Jahrhundertwende herum den Begriff Vakzination – nach dem lateinischen Wort für Kuh (vacca) – für die von Jenner entwickelte Methode [2].

Die Impfung setzte sich in Europa schnell durch und schützte in weiterer Folge Menschen weltweit vor den potenziell tödlichen Pocken. In Österreich trug vor allem Kaiserin Maria Theresia zur Verbreitung der Pockenimpfung bei: Sie ließ drei ihrer Kinder impfen und errichtete ein "Inokulationshaus" [3]. Im Jahr 1800 fand in Brunn am Gebirge (Niederösterreich) die erste Massenimpfung Kontinentaleuropas statt und ein Jahr später wurde in Wien das erste „Schutzpockenimpfungs-Hauptinstitut“ gegründet. Im Jahr 1807 führten Bayern und Hessen eine Impfpflicht gegen Pocken ein, ab 1874 galt in ganz Deutschland die Impfpflicht für Kinder, ansonsten drohten Geld- und Haftstrafen.
Im 20. Jahrhundert führten die Entdeckung von Krankheitserregern und die Erfahrungen mit der Pockenimpfung zur Entwicklung weiterer Impfstoffe. Allen voran sind hier Louis Pasteur und Robert Koch zu nennen. Pasteur gilt als Erfinder der Tollwut-Impfung, und gemeinsam mit Koch entdeckte er außerdem den Erreger des Milzbrands, gegen den sie ebenfalls einen Impfstoff entwickelten. Ein weiterer Meilenstein war die Entwicklung von Impfstoffen gegen Diphterie und Tetanus durch Emil van Behring und Paul Ehrlich.
Seit diesen bahnbrechenden Entwicklungen zählen Impfungen zu den erfolgreichsten Gesundheitsmaßnahmen, die je erfunden wurden. Die letzten Fälle der Pocken wurden Mitte der 1970er-Jahre gemeldet, und 1980 verkündete die WHO die weltweite Ausrottung der Pocken. Heute schützen uns Impfungen auch vor vielen anderen Krankheiten. Laut Schätzungen retten Impfungen weltweit jährlich etwa sechs Millionen Menschenleben [4].
Immunsystem und Impfung
Alle Impfungen basieren auf folgendem Grundprinzip: Unser Immunsystem wird vorbeugend mit dem Impfantigen – einem bestimmten Erreger bzw. Bestandteilen von diesem – bekannt gemacht und dadurch aktiviert. Es werden Antikörper dagegen produziert und Gedächtniszellen gebildet. Bei einer Infektion mit dem echten Erreger erkennt das Immunsystem diesen wieder und kann ihn schnell und effizient bekämpfen.
Damit Impfungen auf diese Weise einen Schutz vor Krankheitserregern bieten können, ist ein intaktes Immunsystem vonnöten. Unser Immunsystem stellt – neben dem Gehirn – eines der komplexesten Systeme des menschlichen Körpers dar. Als biologisches Abwehrsystem schützt es uns vor Bakterien, Viren, Pilzen und Parasiten, mit denen wir laufend zu tun haben. Das Immunsystem des Menschen besteht aus spezialisierten Organen, Zellen und Molekülen. Über Blut und Lymphe zirkulieren die Immunzellen im gesamten Körper und sind auch in den Körpersekreten zu finden.
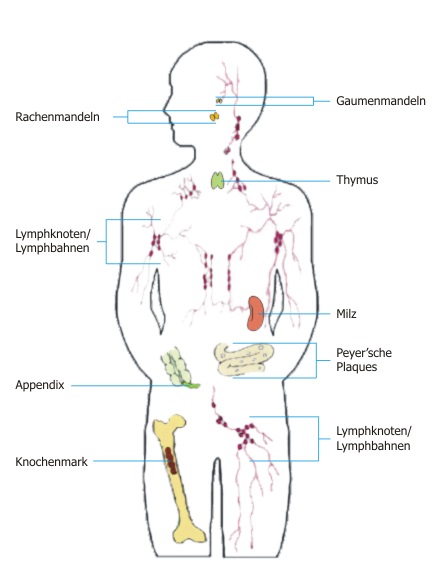
Die Aufgabe des Immunsystems ist es, Krankheitserreger im Körper so rasch wie möglich (I) zu erkennen, (II) zu markieren und (III) zu eliminieren. Dabei muss es zwischen gefährlich und ungefährlich sowie Selbst und nicht-Selbst unterscheiden. Fremdstoffe – wie beispielsweise Schmutzpartikel bei Verletzungen oder Schadstoffe aus der Luft – werden ebenfalls vom Immunsystem entfernt, und auch an der Wundheilung ist es beteiligt. Weiters eliminiert das Immunsystem Zellen des eigenen Körpers, die entartet sind und eine potenzielle Gefahr darstellen, wie beispielsweise Krebszellen.
Zwei Ebenen der Immunabwehr
Das Immunsystem arbeitet prinzipiell auf zwei Ebenen: Das unspezifische (angeborene) Immunsystem verhindert als erster Schutzschild des Körpers das Eindringen von Krankheitserregern und Fremdpartikeln in den Körper bzw. leitet rasch erste Schritte gegen diese ein. Wird diese erste Barriere überwunden, kommt das spezifische (adaptive, erworbene) Immunsystem zum Einsatz. Das unspezifische und das spezifische Immunsystem laufen nicht isoliert voneinander ab, sondern greifen ineinander, um den Körper vor Krankheiten zu schützen [5].
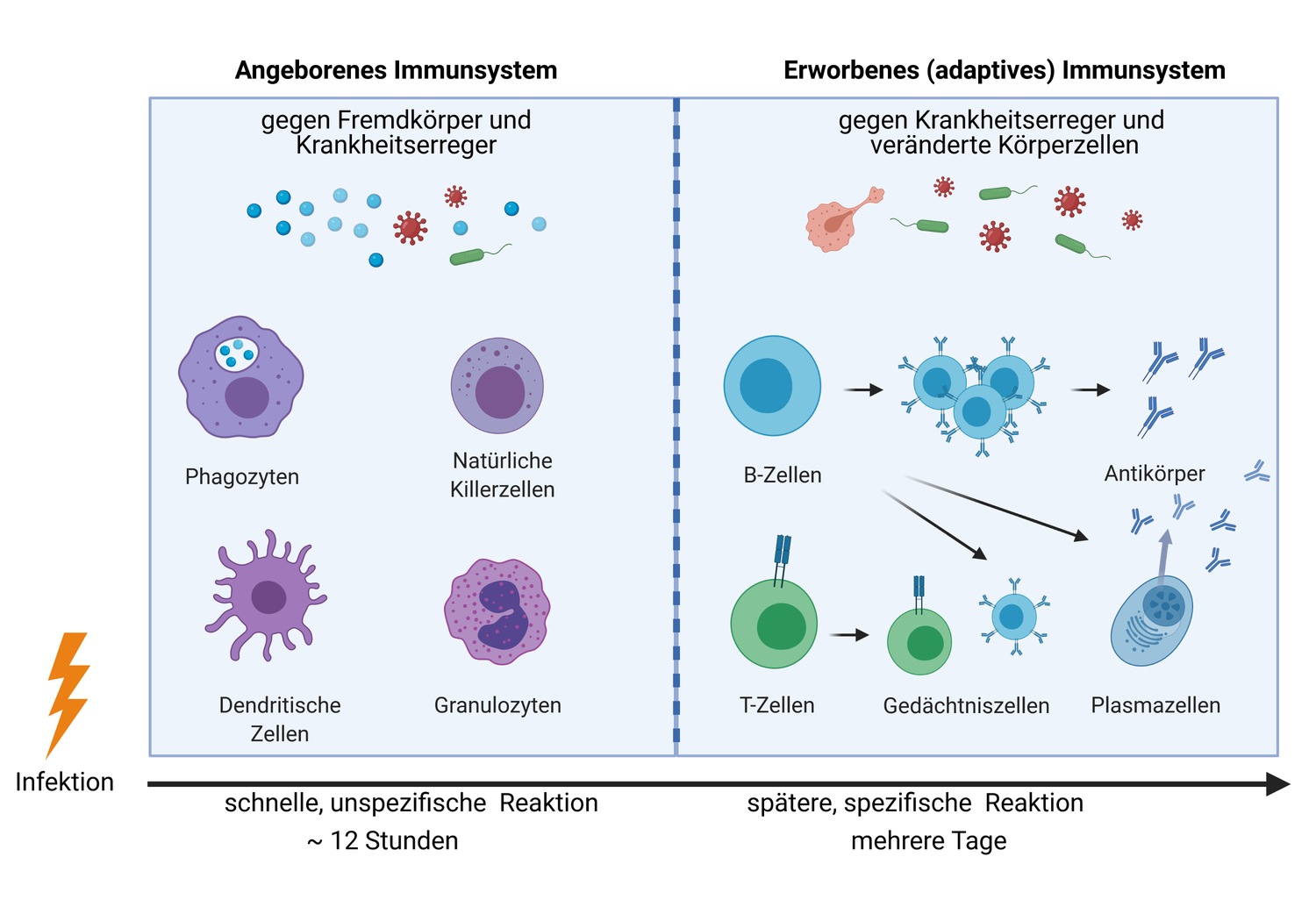
Das unspezifische (angeborene) Immunsystem ist – wie auch sein Name schon verrät – nicht spezifisch für Erreger. Rasch – meist innerhalb von Stunden – setzen hier unspezifische zelluläre und nicht-zelluläre Abwehrmechanismen ein, die komplementär arbeiten – also aufeinander aufbauen und sich ergänzen:
- Mechanische und biochemische Barrieren bilden die erste Verteidigungslinie unseres Körpers gegen Krankheitserreger. Dazu zählt beispielsweise der Säureschutzmantel der Haut, der saure pH-Wert im Magen, Sekrete an der Oberfläche der Schleimhäute sowie die Tränenflüssigkeit. Diese verhindern das Eindringen von Erregern und Partikeln in den Körper.
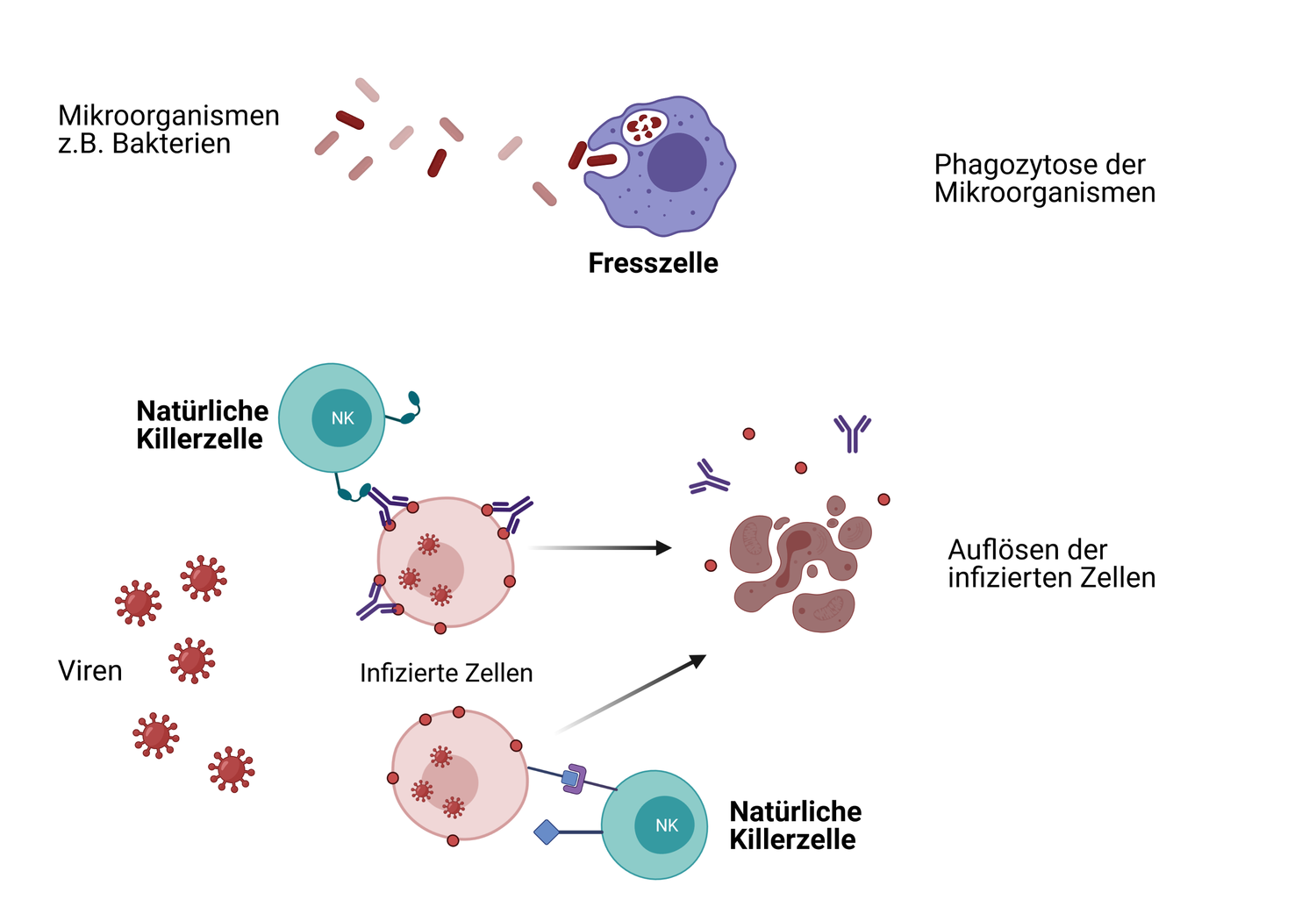
- Werden diese Barrieren jedoch überwunden, kommen verschiedene spezialisierte Zellen zum Einsatz: Fresszellen wie beispielsweise Granulozyten können Erreger durch so genannte Phagozytose aufnehmen und in ihrem Inneren verdauen. Auch natürliche Killerzellen (NK-Zellen) sind in der frühen Phase einer Immunantwort wichtig, da sie virusinfizierte Zellen – und auch Tumorzellen – erkennen und abtöten. Dendritische Zellen, die vor allem in der Haut sitzen, transportieren Antigene über die Lymphe zu den Lymphknoten und stellen so die Verbindung zum spezifischen Teil des Immunsystems dar.
- Auch nicht-zelluläre, gelöste Bestandteile der Immunabwehr wie Proteine oder körpereigene Botenstoffe werden gebildet. Diese steuern die Immunreaktion des Organismus und dirigieren andere Abwehrzellen zum Ort der Entzündung.
Im Gegensatz zum unspezifischen Immunsystem wird das spezifische (= erworbene, adaptive) Immunsystem im Laufe des Lebens stetig erweitert und richtet sich gezielt gegen bestimmte Erreger. Es besitzt große Anpassungsfähigkeit gegenüber neuen oder veränderten Krankheitserregern, muss aber erst aktiviert werden und wirkt nicht sofort ab dem Eindringen eines Erregers.
- Es gibt viele verschiedene Zelltypen der spezifischen Immunabwehr. Hier spielen vor allem zwei Vertreter der weißen Blutkörperchen eine wichtige Rolle: Die B-Zellen und die T-Zellen.
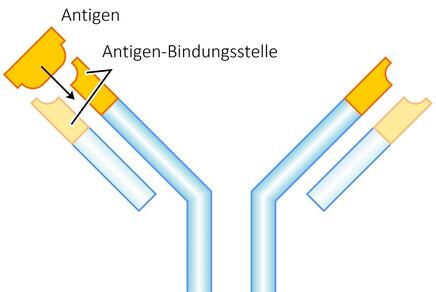
- B-Zellen und T-Zellen sind in der Lage, Antigene – das sind fremde Substanzen wie Zellbestandteile – oder Fremdkörper zu erkennen und gezielt spezifische Abwehrmechanismen dagegen zu entwickeln. Von den B-Zellen werden Antikörper gebildet, welche Antigene erkennen und binden.
- Eine spezifische Immunantwort tritt später ein als eine unspezifische, sie wirkt etwa ab sieben Tage nach dem Auftreten einer Infektion.
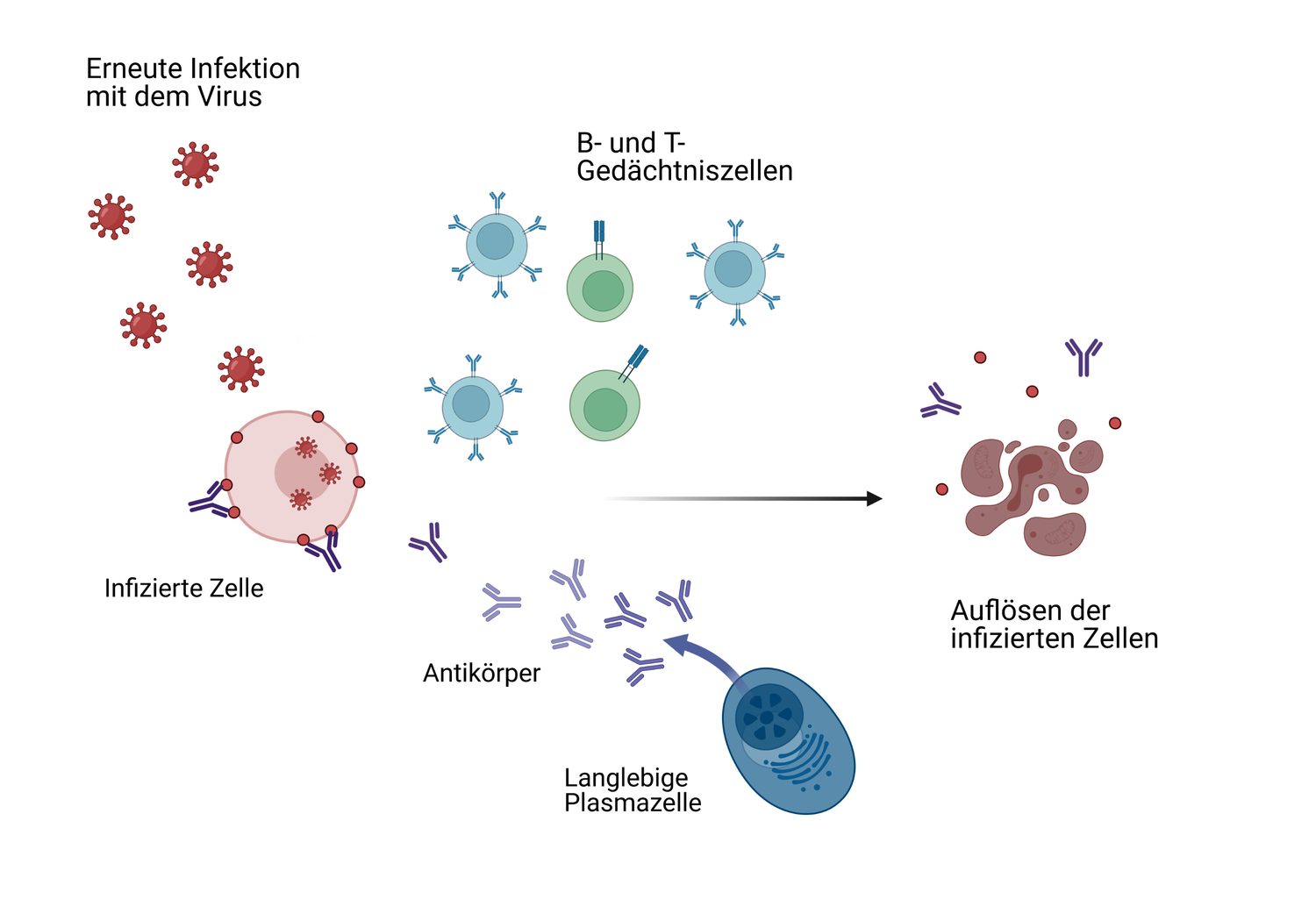
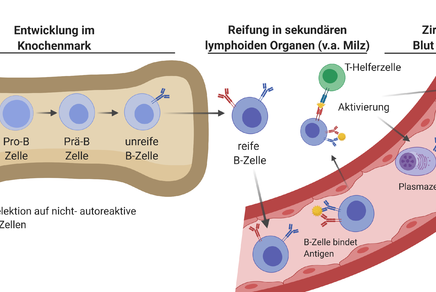
Nur bei einer spezifischen Immunreaktion kann ein immunologisches Gedächtnis aufgebaut werden: Langlebige Plasmazellen, die mehrere Jahre im menschlichen Körper überdauern können, sowie B- und T-Gedächtniszellen „merken“ sich Erreger. Sie reagieren dann im Fall einer erneuten Infektion schneller und besser darauf, sodass der Erreger sofort neutralisiert wird und es zu keinem Ausbruch der Krankheit und Schädigung des Körpers kommt. Meistens bewirkt diese Gedächtnisantwort auch, dass die betroffene Person nicht mehr oder weniger infektiös ist. Dieses Prinzip bildet die Grundlage für das Impfen (Immunisieren).
Arten von Impfstoffen
Als Impfen (= Immunisieren) bezeichnet man allgemein das gezielte Herbeiführen der Immunität gegen einen bestimmten Krankheitserreger. Impfstoffe werden auch Vakzine genannt. Prinzipiell unterscheidet man zwischen aktiver und passiver Immunisierung.
1. Aktive Immunisierung
Die aktive Immunisierung erfolgt entweder in manchen Fällen durch eine Erkrankung selbst oder durch eine Schutzimpfung, und es wird ein langfristiger Schutz gegen eine Infektion aufgebaut. Bei manchen Immunisierungen wirkt der Impfschutz lebenslang, bei anderen muss er aufgefrischt werden. Es ist jedoch von Impfstoff zu Impfstoff unterschiedlich, wie viele Impfdosen benötigt werden und wie lange der Impfschutz anhält. Dies hängt davon ab, wie effizient die Immunreaktion nach einer ersten Impfung ist. Bei der Grippeimpfung verhält es sich hier anders: Da sich der Grippeerreger durch Mutationen laufend verändert, muss der Immunschutz jährlich mit einem neu zusammengesetzten Impfstoff angepasst werden.
Gerade für Kinder werden häufig so genannte Kombinationsimpfstoffe verabreicht, welche die Antigene mehrerer, unterschiedlicher Krankheitserreger enthalten. Somit kann gleichzeitig ein Schutz gegen mehrere Krankheiten herbeigeführt und die Anzahl an Injektionen verringert werden. Zu diesen Impfungen zählt beispielsweise die 6-fach Impfung gegen Diphtherie, Wundstarrkrampf (Tetanus), Keuchhusten, Kinderlähmung, Haemophilus influenzae B und Hepatitis B, welche laut Österreichischem Impfplan (Verlinken) Kindern in den ersten beiden Lebensjahren empfohlen wird.
1.1 Lebendimpfstoffe
Lebendimpfstoffe enthalten vermehrungsfähige Erreger, die jedoch keine krankmachenden Eigenschaften mehr besitzen. Die abgeschwächten Erreger lösen im Körper eine Abwehrreaktion aus, die zu schwachen Krankheitssymptomen führen kann. Beispiele für Lebendimpfstoffe mit abgeschwächten Erregern sind Vakzine gegen Masern, Mumps und Röteln.
1.2 Totimpfstoffe
Totimpfstoffe enthalten abgetötete oder abgeschwächte, nicht vermehrungsfähige Erreger. Auch Impfstoffe, die nur Bestandteile oder einzelne Moleküle eines Erregers enthalten, zählen zu dieser Klasse. Häufig werden für solche Impfstoffe so genannte Adjuvantien benötigt – das sind Hilfsstoffe, die die Immunantwort auf die verabreichte Substanz steigern. Adjuvantien können allerdings Impfreaktionen wie eine Verhärtung an der Einstichstelle oder erhöhte Körpertemperatur hervorrufen. Totimpfstoffe lösen in der Regel schwächere Immunantworten aus als Lebendimpfstoffe und müssen daher aufgefrischt werden. Beispiele für Totimpfstoffe sind Vakzine gegen Hepatitis A und Influenza.
1.3 Genbasierte Impfstoffe
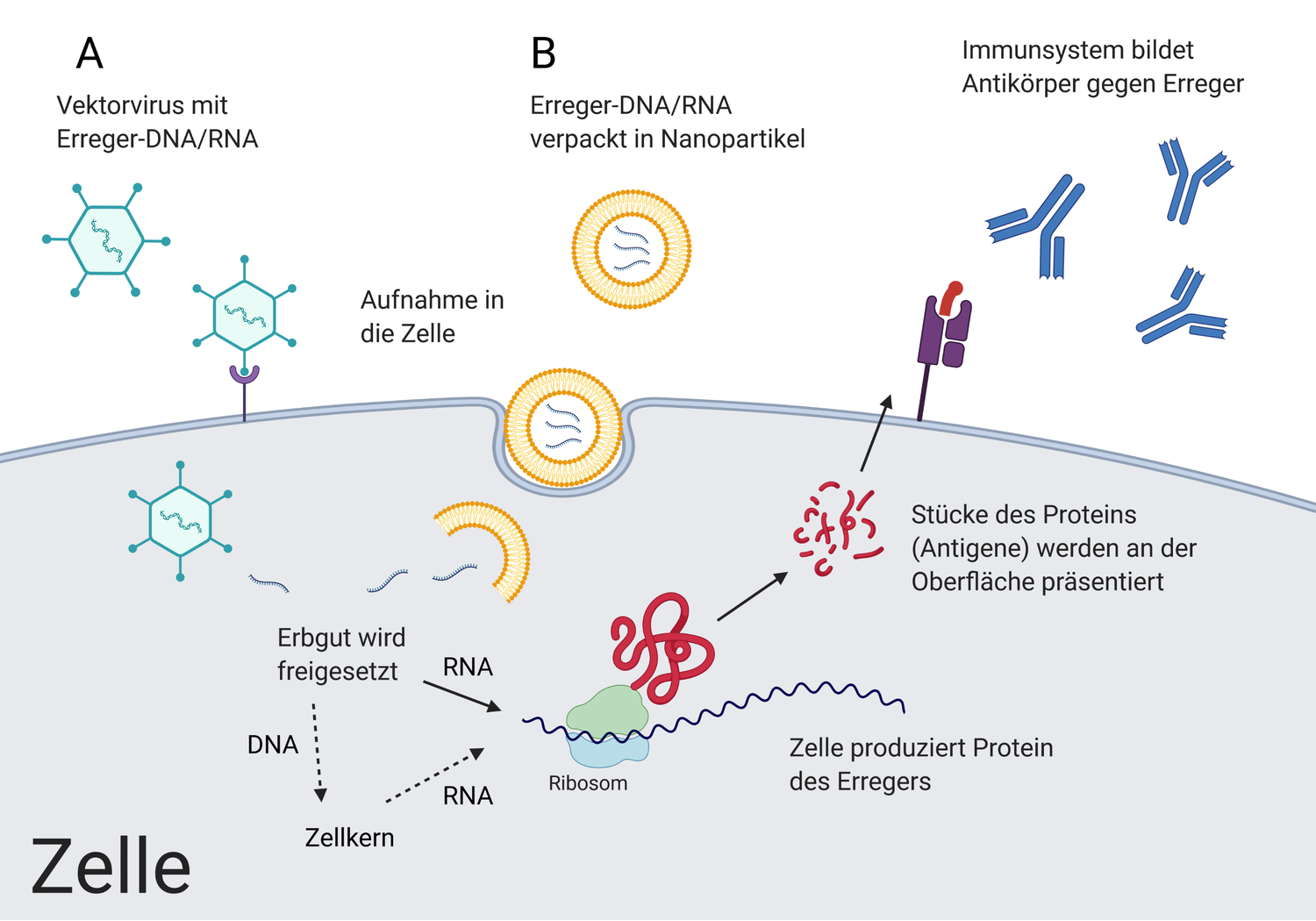
Seit einigen Jahren werden auch neue, genbasierte Impftechnologien eingesetzt. Dabei werden nicht der Krankheitserreger selbst oder Teile davon injiziert, sondern stattdessen ein Teil der genetischen Information des Erregers. Nach dieser Vorlage stellt dann der Körper die Impfantigene selbst her. Zu den genbasierten Impfstoffen zählen Vektorimpfstoffe sowie DNA- und RNA-Impfstoffe (vgl. Abbildung 5). Ihr Herstellungsprozess ist schneller und kostengünstiger als der von Lebend- und Totimpfstoffen.
1.3.1 Vektorimpfstoffe
Das genetische Material, das den Bauplan für ein oder mehrere Antigene des Erregers liefert, wird in so genannte Trägerviren (Vektorviren) eingebracht. Dabei handelt es sich um Viren, die so verändert wurden, dass sie nicht mehr krank machen, aber menschliche Zellen infizieren können. Das gewünschte Genmaterial kann so in den Körper eingeschleust werden: Die Vektorviren heften sich an die Oberfläche ihrer Zielzellen und bringen den Antigen-Bauplan ins Zellinnere ein. Die infizierten Zellen produzieren daraufhin das Erreger-Antigen, und die geimpfte Person entwickelt einen Impfschutz gegen den betreffenden Erreger. Vektor-basierte Impfstoffe wurden bereits zur Bekämpfung des Ebola-Virus zugelassen [6] und kommen auch in der aktuellen Corona-Pandemie zum Einsatz. In Europa war AZD1222 von AstraZeneca/University of Oxford der erste Vektorimpfstoff gegen SARS-Cov-2 [7, 8].
1.3.2 DNA- und RNA-Impfstoffe
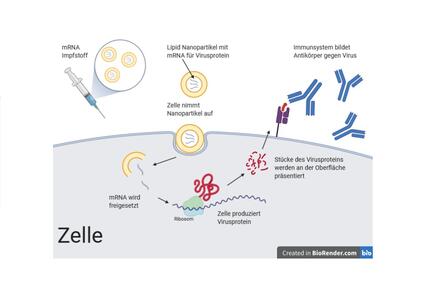
Bei dieser Art von Impfstoffen werden ausgewählte Gene des Erregers in Form von Nukleinsäuren – DNA oder RNA – in den Körper eingebracht. Die Nukleinsäure liegt nicht nackt vor, sondern ist umhüllt – beispielsweise von Lipidnano-Partikeln, die man sich wie kleine, schützende Fetttröpfchen vorstellen kann. DNA oder RNA liefern in den menschlichen Zellen dann den Bauplan für die Herstellung des entsprechenden Proteins. So können beliebige Antigene des Erregers von der Maschinerie des Menschen hergestellt und seine Körperzellen als Impfstofffabriken genutzt werden. Das Immunsystem erkennt die fremden Antigene. Wie bei herkömmlichen Impftechnologien stimulieren diese eine Immunreaktion, sind ansonsten aber harmlos. Die RNA-Impfstoffe BNT162 von BioNTech/Fosun/Pfizer und mRNA-1273 von Moderna/NIAID waren die ersten Impfstoffe am Markt, um den Kampf gegen SARS-CoV-2 aufzunehmen [7, 8].
2. Passive Immunisierung
Eine passive Immunisierung dient dazu, eine bereits bestehende Infektion zu behandeln. Dazu werden dem Körper anstatt des Erregers die Antikörper dagegen und somit „fertige“ Abwehrstoffe geimpft. Diese markieren den Erreger für das Immunsystem, welches ihn unschädlich macht. So können Ausbruch und Verlauf einer Krankheit gemildert werden. Die Antikörper werden vom Körper jedoch abgebaut und bleiben nicht wie langlebige Plasmazellen oder Gedächtniszellen erhalten. Deshalb hält der Schutz nach einer passiven Immunisierung nur wenige Monate an. Passive Immunisierungen gibt es zum Beispiel gegen Tetanus und Tollwut.
Verabreichungsformen von Impfungen
Bei der Verabreichung von Impfstoffen gibt es mehrere Möglichkeiten:
- Injektion: Die meisten aktiven Impfstoffe werden in Form einer Injektion verabreicht: Der Impfstoff wird mit einer Nadel in den Muskel (intramuskulär), unter die Haut (subkutan) oder in die Haut (intradermal) gespritzt. Bei den meisten Impfstoffen ist heute die intramuskuläre Impfung üblich. Als beste Impfstelle gilt hier grundsätzlich der Deltamuskel am Oberarm, bei Babys auch der Oberschenkel. In den Gesäßmuskel wird heute nicht mehr injiziert, da dieser von einer mehr oder weniger dicken Fettschicht bedeckt ist und von wichtigen Nervenbahnen durchzogen wird.
- Bei Schluckimpfungen erfolgt die Verabreichung oral, und der Körper nimmt den Impfstoff anschließend über den Magen-Darm-Trakt auf. Die Impfung gegen Kinderlähmung (Polio) kann beispielsweise im Fall des Lebendimpfstoffs als Schluckimpfung verabreicht werden. Heute wird allerdings eher zur Injektion eines Totimpfstoffs gegen Polio geraten, da hier weniger Komplikationen auftreten. Auch gegen Rotaviren und Cholera gibt es Schluckimpfungen.
- Die Spray-Impfung und das Inhalieren stellen relativ neue Entwicklungen dar. Der Impfstoff gelangt in beiden Fällen über die Atemwege in den Körper. Für den herkömmlichen Impfstoff gegen Grippe (Influenza) gibt es bereits eine vergleichbar wirksame Nasenspray-Variante.
- An einer Verabreichung über die Haut mittels Impfpflaster wird ebenfalls gearbeitet [9, 10]. In Tests schnitt ein Grippe-Pflaster mit Mikronadeln bereits genauso gut ab wie die Spritze [9, 10].
- Auch an essbaren Impfstoffen aus gentechnisch veränderten Pflanzen wird gearbeitet. So sollen beispielsweise Bananen, Kartoffeln oder Tomaten direkt einen Wirkstoff bilden, der dann durch den Verzehr ebendieser verabreicht wird. An Pflanzen als Produktionsstätten für Impfstoffe, welche dann aus den Pflanzen gewonnen werden können, wird ebenfalls geforscht [11].
Aktivierung des Immunsystems durch Impfung
Die Abläufe nach einer Impfung im Körper ähneln der Reaktion des Immunsystems bei einer „echten“ Infektion. Ziel einer Impfung ist es, die körpereigene Immunabwehr zu mobilisieren. Die Produktion von Antikörpern gegen den Erreger soll angekurbelt und sowohl langlebige Plasmazellen als auch Gedächtniszellen sollen gebildet werden. Bei einer Infektion mit dem „echten“ Erreger trifft der Körper dann bereits zum wiederholten Mal auf das Antigen. Er ist schon mit Antikörpern bzw. mit Gedächtniszellen gewappnet und kann schnell und effizient dagegen ankämpfen.
Bei der gängigsten Methode des Impfens, der intramuskulären Injektion, gelangt der Impfstoff über die feinen Gefäße, die den Muskel durchziehen, nach und nach in die Blutbahn. Der Impfstoff wird langsam abgegeben, was ihn gut verträglich macht. Bei subkutaner und intradermaler – und zu einem bestimmten Anteil auch bei intramuskulärer – Injektion hingegen spielt eine bestimmte Gruppe der weißen Blutzellen eine entscheidende Rolle: die dendritischen Zellen. Diese Wächterzellen haben die Aufgabe, die Erreger bzw. Teile davon aufzuspüren, aufzunehmen und zu den umliegenden Lymphknoten zu transportieren. Dort wird eine ganze Kaskade von Reaktionen ausgelöst, was zur Produktion von Antikörpern gegen den Erreger führt. Dendritische Zellen befinden sich in großer Dichte in der Haut, aber auch in den Schleimhäuten der Atemwege und in der Lunge. Daher sind sie auch bei der Impfstoff-Applikation über die Haut und über die Schleimhäute – wie beispielsweise die der Atemwege und des Magens – wichtig. Im Muskel dagegen kommen dendritische Zellen in deutlich geringerer Anzahl vor. Daher gibt es Überlegungen, von der intramuskulären Injektion, bei der dendritische Zellen weniger involviert sind, generell auf subkutane oder intradermale Anwendung umzusteigen.
Es gibt aber auch eine organspezifische Immunantwort, besonders bei den Schleimhäuten in der Lunge oder im Darm. Deshalb versucht man aktuell auch, Impfstoffe zu entwickeln, die über diesen Weg aufgenommen werden. Beispiele dafür sind ein Nasenspray gegen Influenza oder eine Schluckimpfung gegen Rotaviren/Cholera. Da so der Infektionsweg des Erregers nachgeahmt wird und die Zielorgane des Impfstoffs auch die der Erreger sind, schützen Impfungen in dieser Form optimal.
Impfreaktion, Nebenwirkung, Komplikation oder Impfschaden?
Zwischen Impfreaktionen und Nebenwirkungen einer Impfung sowie Komplikationen und Impfschäden muss klar unterschieden werden [12, 13]. Reaktionen können prinzipiell nicht nur auf Erreger-Bestandteile des Impfstoffs bzw. auf dessen Nukleinsäure, sondern auch auf andere Inhaltsstoffe – wie beispielsweise Adjuvantien, also Bestandteile des Impfstoffs, die selbst nicht wirksam sind, aber die Wirkung des Hauptbestandteils unterstützen – erfolgen.
- Impfreaktionen sind relativ häufig und normal. Darunter versteht man harmlose Beschwerden, die im Rahmen der Immunantwort auf eine Impfung auftreten können. Bis zu einem gewissen Grad sind diese sogar wünschenswert, da sie zeigen, dass sich der Organismus mit dem Impfstoff auseinandersetzt. Zu den Impfreaktionen zählen Lokalreaktionen wie Brennen oder das Entstehen einer Rötung an der Einstichstelle. Auch Reaktionen wie (leichtes) Fieber, Abgeschlagenheit oder grippeartige Beschwerden können auftreten. In seltenen Fällen kann die Erkrankung, gegen die geimpft wurde, in abgeschwächter Form als sogenannte Impfkrankheit (z.B. Impfmasern) ausbrechen. Die Symptome sollten jedoch innerhalb weniger Tage wieder abklingen.
- Als Nebenwirkung hingegen wird laut Arzneimittelgesetz eine „schädliche und unbeabsichtigte Reaktion auf das Arzneimittel“ bezeichnet [13].
- Von einer schwerwiegenden Nebenwirkung spricht man, wenn diese „tödlich oder lebensbedrohend ist, eine stationäre Behandlung oder deren Verlängerung erforderlich macht, zu bleibender oder schwerwiegender Behinderung oder Invalidität, einer kongenitalen Anomalie oder einem Geburtsfehler führt“ [12, 13].
- Auch von Impfkomplikationen hört man öfter. Dabei handelt es sich um eine Rarität, damit sind beispielsweise allergische Reaktionen gemeint, die etwa mit einer Häufigkeit von 1 pro 500.000 bis 1 Million Geimpfte auftreten, oder Anaphylaxie bei 1 bis 1,5 Millionen verimpfter Dosen [13].
- Als Impfschaden wird eine durch eine Impfung verursachte schwere, bleibende Behinderung definiert. Dabei handelt es sich um einen rechtlichen und nicht um einen medizinischen Begriff.
Prinzipiell führen Erkrankungen, gegen die geimpft werden kann, selbst weitaus häufiger zu schweren Komplikationen und bleibenden Schäden als die Impfungen dagegen [14].
In Österreich erstellt das Gesundheitsministerium gemeinsam mit dem nationalen Impfgremium, einer unabhängigen ExpertInnenkommission, jährlich einen Impfplan. Dieser richtet sich an ÄrztInnen sowie alle Interessierten und gibt einen Überblick über aktuelle zur Verfügung stehende und empfohlene Impfungen zum Schutz vor Infektionskrankheiten. Derzeit gibt es für 16 Impfungen eine nationale Impfempfehlung, der Großteil davon wird im Kindesalter verabreicht [15].
Wir bedanken uns recht herzlich bei Dr. Nicole Boucheron von der Medizinischen Universität Wien für die fachliche Unterstützung bei diesem Artikel!
as, cp, 10.12.2021
Quellenangaben
[1] Plotkin S. A., Mortimer E. A. (1988). Vaccines. Philadelphia, PA: Saunders.
[2] I. Bailey: Edward Jenner (1749–1823): naturalist, scientist, country doctor, benefactor to mankind. In: Journal of Medical Biography. Band 4, Nummer 2, Mai 1996, S. 63–70. PMID 11616266.
[3] Flamm, H. and Vutuc, C. (2010). Geschichte der Pocken-Bekämpfung in Österreich. Wiener Klinische Wochenschrift, 122(9-10), 265–275. doi:10.1007/s00508-010-1379-0
[4] Ehreth J. The value of vaccination: a global perspective. Vaccine. 2003 Oct 1;21(27-30):4105-17. doi: 10.1016/s0264-410x(03)00377-3. PMID: 14505886.
[5] Marshall JS, Warrington R., Watson W. and Kim HL.: An introduction to immunology and immunopathology. Allergy Asthma Clin Immunol. 2018;14(Suppl 2):49. Published 2018 Sep 12. doi:10.1186/s13223-018-0278-1
6] Henao-Restrepo AM, Camacho A., Longini IM et al. Efficacy and effectiveness of an rVSV-vectored vaccine in preventing Ebola virus disease: final results from the Guinea ring vaccination, open-label, cluster-randomised trial (Ebola Ca Suffit!). Lancet 2017, 389, (10068), 505-518.
[7] Vrba SM, Kirk NM, Brisse ME et al.: Development and Applications of Viral Vectored Vaccines to Combat Zoonotic and Emerging Public Health Threats. Vaccines (Basel). 2020;8(4):680. Published 2020 Nov 13. doi:10.3390/vaccines8040680
[8] Ura T., Yamashita A., Mizuki N. et al.: New vaccine production platforms used in developing SARS-CoV-2 vaccine candidates. Vaccine. 2021;39(2):197-201. doi:10.1016/j.vaccine.2020.11.054
[9]: Rouphael NG, Paine M., Mosley R. et al.: The safety, immunogenicity, and acceptability of inactivated influenza vaccine delivered by microneedle patch (TIV-MNP 2015): a randomised, partly blinded, placebo-controlled, phase 1 trial. The Lancet, Vol. 390, Issue 10095, p.649-658, August 12, 2017
[10]: Rodgers AM, Cordeiro AS and Donnelly RF: Technology update: dissolvable microneedle patches for vaccine delivery. Med Devices (Auckl). 2019;12: 379-398. Published 2019 Sep 19. doi:10.2147/MDER.S198220
[11] Kurup VM and Thomas J.: Edible Vaccines: Promises and Challenges. Mol Biotechnol. 2020;62(2):79-90. doi:10.1007/s12033-019-00222-1
[13] AGES, Medizinmarktaufsicht – BASG, Tucek B.: Impfnebenwirkungen versus Impfschäden (2020).
[14] Öffentliches Gesundheitsportal Österreichs: Nebenwirkungen von Impfungen.
Ansprechpartner:
- Alexandra Schebesta