Newsletter
Stammzellen: Hoffnungsträger und Stein des Anstoßes
, Bild: Pixabay, CCO
Stammzellen gelten in der Medizin als große Hoffnungsträger für die Therapie von Krankheiten. Was sind Stammzellen genau, und welche Möglichkeiten haben sie bereits eröffnet? Ein kurzer Überblick zu den Grundlagen, dem Status Quo und konkreten Anwendungen der Stammzellforschung sowie ethische Fragen rund um dieses Thema.
Stammzellen: Seltene Alleskönner
Stammzellen sind seltene Alleskönner unter den Zellen und bilden das natürliche Reservelager unseres Körpers. Sie haben die Fähigkeit zur Selbsterneuerung und können durch symmetrische Zellteilung wieder Stammzellen bilden. Stammzellen können aber auch den Weg der Differenzierung einschlagen und durch asymmetrische Teilung zu Stammzellen mit geringerem Entwicklungspotential oder zu spezialisierten Zellen – wie z.B. Blut-, Herz-, Muskel- oder Leberzellen – ausreifen. Der Differenzierungsprozess läuft schrittweise unter Einwirkung verschiedener Botenstoffe und Signale aus der Umgebung der Zelle ab.
Aus den Stammzellen gehen im Laufe der Embryonalentwicklung alle verschiedenen Zelltypen und Gewebe eines Organismus hervor. Aber auch im Erwachsenenalter werden Stammzellen benötigt, denn sie sorgen dafür, dass abgestorbene Zellen erneuert werden. Sie sind beim Menschen unverzichtbar für die Erhaltung von Organen und Geweben, die sich ständig erneuern – wie beispielsweise das Blut, die Haut oder der Darm. Im Knochenmark – dem Sitz der Blutstammzellen - werden jeden Tag mehrere Milliarden neuer Blutzellen produziert [1]. Muskelzellen müssen im Gegensatz dazu nicht laufend erneuert werden. Bei körperlicher Anstrengung jedoch können sie geschädigt werden und müssen danach auch wieder aufgebaut werden.
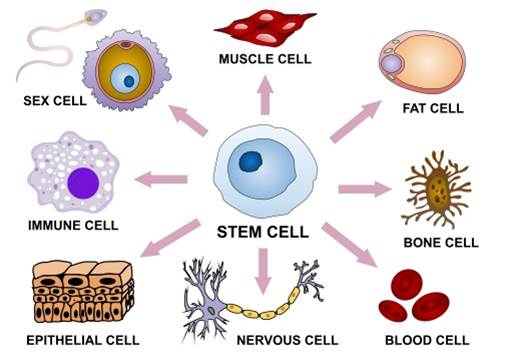
Einteilung der Stammzellen nach ihrem Differenzierungspotential
Während des Vorgangs der Differenzierung reifen Stammzellen schrittweise über die Zwischenstufe von sogenannten Vorläuferzellen heran. Vorläuferzellen sind bereits für eine bestimmte Richtung determiniert, und ihr weiterer Entwicklungsweg ist festgelegt. Aus ihnen entstehen in weiterer Folge spezialisierte Zelltypen des jeweiligen Ursprungsgewebes. So gehen beispielsweise aus neuronalen Vorläuferzellen Nervenzellen hervor, aus glialen Vorläuferzellen jedoch Gliazellen, die die Nervenstränge umhüllen. Vorläuferzellen haben nur mehr eine begrenzte Fähigkeit zur Selbsterneuerung. Wenn die Spezialisierung eines Zelltyps abgeschlossen ist – die Zelle also ausdifferenziert ist - geht auch ihre Fähigkeit zur Zellteilung verloren.
Stammzellen können anhand ihres Differenzierungspotentials eingeteilt werden. Beim Menschen werden folgende Stammzellen unterschieden:
- Ganz oben in der Hierarche steht die befruchtete Eizelle. Sie ist totipotent (=omnipotent) und hat die Fähigkeit, einen gesamten Organismus auszubilden. Aus dem befruchteten Ei, auch Zygote genannt, gehen beim Menschen sowohl der Embryo als auch ein Teil der Plazenta hervor. Die Fähigkeit, wirklich einen gesamten Menschen bilden zu können, geht bereits nach den ersten Zellteilungen endgültig verloren und dauert nur bis ins 8-Zell-Stadium an.
- Etwa fünf Tage nach der Befruchtung entwickelt sich die Blastozyste, die sich in der Gebärmutter einnistet. Aus diesem Stadium werden sogenannte embryonale Stammzellen (ES-Zellen) gewonnen. Aus embryonalen Stammzellen kann sich jedes menschliche Gewebe entwickeln, aber kein vollständiger Mensch mehr. Daher bezeichnet man sie als pluripotent.
- Durch weitere Differenzierung entstehen adulte Stammzellen, die multipotent sind. Sie können sich üblicherweise nur mehr in die Zelltypen jenes Gewebes/Organs entwickeln, in dem sie lokalisiert sind. Beispielsweise zählen dazu neuronale Stammzellen in bestimmten Regionen des Gehirns, retinale Stammzellen in der Netzhaut, mesenchymale Stammzellen in Knochenmark, Fettgewebe und Haut oder hämatopoetische Stammzellen im Blut. Da jede Zelle im Körper eine begrenzte Lebensdauer hat, sind adulte Stammzellen notwendig, um absterbende Zellen zu ersetzen und somit die Funktionsfähigkeit von Organen und Geweben aufrecht zu erhalten.
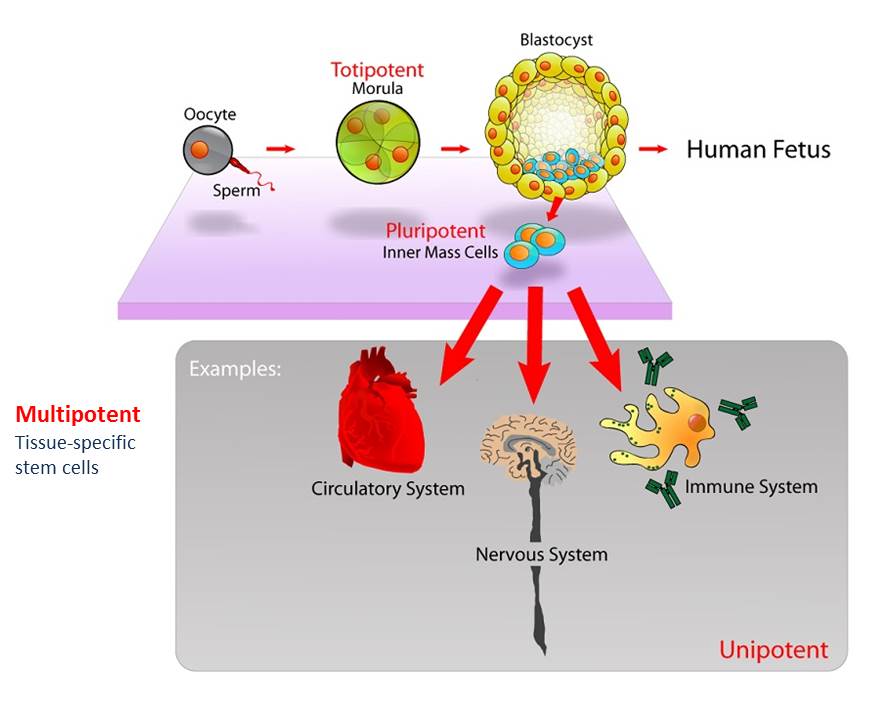
Embryonale Stammzellen und induzierte pluripotente Zellen
Ziel der Stammzellforschung ist es, neue Strategien zu entwickeln, um erkrankte, verletzte oder vorzeitig abgenützte Gewebe reparieren oder ersetzen zu können. Dies soll durch die Transplantation von Stammzellen oder daraus gezüchteten, reiferen Zellen geschehen. Erste Erfolge konnten auf dem Gebiet des Tissue Engineering – der Herstellung biologischer Gewebe durch die gerichtete Kultivierung von Zellen – mit Stammzellen bereits erzielt werden. [2] In der heutigen Stammzellforschung kommen vor allem zwei Arten von Stammzellen zum Einsatz: Embryonale Stammzellen (ES-Zellen) und induzierte Pluripotente Stammzellen (iPS).
- Embryonale Stammzellen (ES-Zellen): Eine befruchtete menschliche Eizelle (Zygote) entwickelt sich durch Zellteilung innerhalb von vier Tagen zu einem Embryo von etwa 0,15 Millimetern Größe (Blastozystenstadium). EmbryonaleStammzellen werden aus der inneren Zellmasse (Embryoblast) von Blastozysten gewonnen. Sie sind in vitro praktisch unbegrenzt vermehrbar und können sich (zumindest theoretisch) in der Kulturschale im Labor in alle rund 200 verschiedenen Zelltypen des Körpers entwickeln. Aus ihnen kann somit jedes Gewebe des menschlichen Körpers hervorgehen. Ein vollständiges Lebewesen kann aus ihnen jedoch nicht mehr entstehen. Im Jahr 1998 gelang es erstmals, embryonale Stammzellen aus übrigen Embryonen von Fruchtbarkeitskliniken zu kultivieren. [3] Auch heute noch werden ES-Zellen hauptsächlich aus überzähligen Embryonen, die im Zuge von künstlichen Befruchtungen entstanden sind, gewonnen. Eine weitere mögliche Quelle für ES-Zellen sind auch Blastozysten, die durch therapeutisches Klonen hergestellt wurden. Dabei wird der Kern aus einer Körperzelle des Patienten/ der Patientin mit einer entkernten Eizelle verschmolzen. Daraus entwickeln sich Embryonen, aus denen sich nach wenigen Tagen embryonale Stammzellen gewinnen lassen. Bei der Gewinnung der Stammzellen wird der Embryo zerstört, somit entwickelt sich kein geklontes lebensfähiges Individuum.
- Induzierte Pluripotente Stammzellen (iPS-Zellen): Im Jahr 2007 gelang es mehreren Forschungsgruppen unabhängig voneinander, adulte menschliche Zellen so umzuprogrammieren, dass sie Eigenschaften von embryonalen Stammzellen annahmen. [4] Diese Zellen werden induzierte pluripotente Stammzellen oder iPS-Zellen genannt. Schon 2012 wurde dafür der Nobelpreis für Medizin an Shinya Yamanaka und John Gurdan verliehen. Zum Reprogrammieren der adulten Zellen wurden mehrere Kontrollgene (meist Oct4, Sox2, Kfl4 und Myc) mit Hilfe von viralen Transportvehikeln, sogenannten Vektoren, in die Zellen eingeschleust. Diese werden in die zelleigene DNA eingebaut und bewirken, dass das embryonale Programm der Zelle wieder angeschaltet wird. Verschiedenste Gewebe konnten so zu iPS-Zellen umprogrammiert werden. Diese Zellen haben die Fähigkeit zur unbegrenzten Teilung und können sich wieder in alle drei Keimblätter entwickeln. Unter Zugabe spezifischer Wachstumsfaktoren konnten iPS-Zellen in verschiedenste Zelltypen wie beispielsweise Nerven-, Muskel-, Leber- oder Fettzellen differenziert werden.
Adulte Stammzellen
Im menschlichen Körper sind von Geburt an bis ins hohe Alter sogenannte adulteStammzellen zu finden. Diese kommen im Knochenmark, im Blut und in vermutlich allen Organen vor, jedoch in geringer Menge. Adulte Stammzellen haben ein limitiertes Entwicklungspotential, d.h. sie sind nicht mehr so flexibel wie embryonale Stammzellen. Aus ihnen entstehen nur noch Zelltypen ihres jeweiligen Organs, sie sind somit multipotent. Adulte Stammzellen ersetzen die laufend absterbenden Zellen in Geweben und ermöglichen so unter anderem die Wundheilung. Sie wurden bisher in vielen Organen und Geweben identifiziert, die Charakterisierung von Zellen mit Stammzell-Eigenschaften, die nur in geringer Anzahl vorkommen, ist jedoch ein langwieriger Forschungsprozess. Ihre begrenzte Lebensdauer macht es schwierig, adulte Stammzellen in der Kulturschale zu züchten.
Die adulten Stammzellen des menschlichen Knochenmarks (hämatopoietische Stammzellen) sind bereits relativ gut untersucht und kommen schon routinemäßig bei der Knochenmarkstransplantation zum Einsatz. Es ist gelungen, menschliche Knochenmark-Stammzellen zum „Redifferenzieren“ zu bringen und sie „umzuprogrammieren“: Unter entsprechenden Kulturbedingungen können sich daraus Zellen einer anderen Linie, wie beispielsweise reife Nervenzellen, entwickeln. Dieser Ansatz könnte für PatientInnen mit neuronalen Erkrankungen, wie beispielsweise Parkinson, hilfreich sein. Im Tierversuch ist das Umprogrammieren von Stammzellen bereits auch mit Stammzellen anderer Gewebe gelungen. Die Bedingungen und Faktoren, die ein solches Umprogrammieren von adulten Stammzellen ermöglichen, werden derzeit intensiv erforscht. Es besteht die große Hoffnung, adulte Stammzellen einmal als Alternative zu embryonalen Stammzellen nutzen zu können.
Als relativ neue und vielseitige Quelle verschiedener adulter Stammzellen gilt das Nabelschnurblut. Auch im Fruchtwasser wurden bereits Stammzellen entdeckt, die die Eigenschaften adulter Stammzellen besitzen. Neue Forschungsarbeiten zeigen, dass rund 1% aller Zellen im Fruchtwasser Stammzell-Eigenschaften aufweisen.
Vor-und Nachteile verschiedener Stammzell-Typen, ethische Bedenken
- ES-Zellen: Der große Vorteil von ES-Zellen gegenüber anderen Stammzellen ist eindeutig ihre Pluripotenz. Ihr immenses Potential liegt darin, daraus sämtliche Zellarten, die für Therapien benötigt werden, im Labor züchten und dem/r Patienten/in implantieren zu können. Die Herstellung der gewünschten Zelltypen in vitro in der Kulturschale ist allerdings sehr schwierig und jahrelange Forschungsarbeiten sind nötig, um die geeigneten Kulturbedingungen dafür überhaupt zu finden. Die Forschung an embryonalen Stammzellen ist außerdem ethisch umstritten, da Embryonen verbraucht werden, die theoretisch das Potenzial haben, einen vollständigen Menschen hervorzubringen. In diesem Zusammenhang werden häufig Fragen diskutiert wie: Wann beginnt das Leben? Welchen rechtlichen Status hat ein Embryo? Gibt es Gründe, die eine verbrauchende Embryonenforschung rechtfertigen? Deshalb gilt es sorgfältig abzuwägen zwischen der Würde und dem Schutz jedes menschlichen Individuums und der Heilung schwerster, bislang meist unheilbarer Krankheiten.
- iPS-Zellen: iPS-Zellen sind im Gegensatz zu embryonalen Stammzellen ethisch weniger bedenklich, da dabei kein Embryo hergestellt oder verbraucht wird. iPS-Zellen müssen allerdings noch gründlich untersucht und getestet werden, um ihr Potential voll ausschöpfen und eventuell damit verbundene Risiken einschätzen zu können.
- Adulte Stammzellen: Der große Vorteil bei der Verwendung von adulten Stammzellen zu Therapiezwecken ist der, dass sie den PatientInnen selbst entnommen werden können und dafür keine Embryonen verbraucht werden müssen (daher ethisch unbedenklich). Im Falle einer Transplantation werden die adulten Stammzellen des Patienten/der Patientin nicht abgestoßen. Im Vergleich zu embryonalen Stammzellen jedoch haben adulte Stammzellen nur ein sehr eingeschränktes Entwicklungspotential und lassen sich im Labor nicht unbegrenzt vermehren. Ihre Identifizierung in den verschiedenen Geweben und Organen ist sehr aufwändig, da sie nur in geringer Menge vorhanden sind.
Rechtliche Situation
Ob menschliche Embryonen für die Gewinnung embryonaler Stammzellen extra hergestellt bzw. geklont werden dürfen, ist rechtlich in Europa unterschiedlich geregelt. Zwar gibt es EU-weite Richtlinien, jedoch können diese in den einzelnen Ländern unterschiedlich ausgelegt werden, und so steht es im Prinzip jedem Land frei, über die Verwendung und Handhabung von Stammzellen zu entscheiden.
In Österreich gibt es keine eindeutige Regelung zur Gewinnung, Einfuhr oder Verwendung von embryonalen Stammzellen. Die Reglementierungen zur Stammzellforschung wurden aus dem Fortpflanzungsmedizingesetz (FMedG, letzte Änderung 2015) abgeleitet, welches Bestimmungen für die „Verwendung, Untersuchung und Behandlung von Samen, Eizellen und entwicklungsfähigen Zellen“ enthält. So gilt in Österreich ein Verbot der Forschung mit menschlichen Embryonen. Die Gewinnung von embryonalen Stammzellen aus Embryonen, die bei künstlichen Befruchtungen übrig bleiben, ist verboten. Die Forschung an embryonalen Stammzellen wurde bisher noch nie finanziell gefördert. Nach dem österreichischen Fortpflanzungsmedizingesetz dürfen entwicklungsfähige Zellen, also Embryonen, nicht für andere Zwecke als für die medizinische Fortpflanzung verwendet werden. Forschung mit pluripotenten ES-Zellen, die in zulässiger Weise bereits entnommen und aus dem Ausland importiert wurden, ist in Österreich allerdings nicht verboten. Hier gibt es somit einen gewissen Graubereich. Forschen an iPS ist in Österreich – wie in vielen anderen Ländern – erlaubt.
In Deutschland verbietet das Embryonenschutzgesetz die Gewinnung von menschlichen embryonalen Stammzellen aus Embryonen. Es gibt allerdings eine Ausnahmeregelung, die den Import und die Forschung mit embryonalen Stammzelllinien, die vor dem 01.05.2007 gewonnen wurden, in Ausnahmefällen toleriert.
Das derzeitige Recht in den USA sieht kein Verbot der Entnahme von Stammzellen aus menschlichen Embryonen vor, wobei jeder Bundesstaat eigenständig entscheiden kann.
Im Menschenrechtsübereinkommen zur Biomedizin des Europarates wird die Erzeugung menschlicher Embryonen für Forschungszwecke ausdrücklich verboten. Außerdem ist es nicht erlaubt, ein menschliches Lebewesen zu erzeugen, das mit einem anderen genetisch identisch ist. Das Übereinkommen wurde aber noch nicht von allen Mitgliedsstaaten unterzeichnet.
In Großbritannien ist die Forschung an menschlichen Embryonen innerhalb der ersten 14 Tage (ca. 1 mm Größe) zu bestimmten Zwecken erlaubt. Dabei stehen das therapeutische Klonen und speziell die Stammzell-Technologie im Mittelpunkt. Aber auch therapeutisches Klonen soll dort nur mit den Körperzellen des/der PatientIn, der/die das gezüchtete Gewebe benötigt, möglich sein.
Anwendungen
Ziel der Stammzellforschung ist es, neue Strategien zu entwickeln, um erkrankte, verletzte oder vorzeitig abgenützte Gewebe zu reparieren oder zu ersetzen. Dies soll durch die Transplantation von Stammzellen oder daraus gezüchteten, reiferen Zellen geschehen. Erste Erfolge wurden bereits erzielt.
Zellersatztherapien
Die Fähigkeit von Stammzellen, verschiedene Gewebe bzw. Organe aufzubauen, weckt große Hoffnungen, in PatientInnen selbst fehlende Zelltypen nachwachsen zu lassen – z.B. durch lokale Injektion von Stammzellen – bzw. die benötigten Zellen im Labor zu züchten und dem Patienten/der Patientin zu implantieren. Beim Menschen werden routinemäßig schon Blutstammzellen aus dem Knochenmark oder aus dem Blut bei Krebspatienten nach Chemo- oder Strahlentherapien, bei der Blutzellen zerstört werden, eingesetzt. Auch zur Behandlung von Leukämie (Blutkrebs) werden diese verwendet. Das Knochenmark dafür kann entweder vom Patienten/der Patientin selbst (vor der Behandlung entnommen, autologe Transplantation) oder von einem Spender/einer Spenderin (allogene Transplantation) stammen. Es besteht große Hoffnung, Krankheiten wie Rheuma, Diabetes, Herzdefekte, verschiedene Bluterkrankungen, Parkinson, Alzheimer und Multiple Sklerose einmal mithilfe von Stammzelltherapien heilen zu können. In Tierversuchen ist dies bereits teilweise gelungen.
Tissue Engineering - Regenerative Medizin
Die Methode des Tissue Engineering (Gewebezüchtung) stellt ein weiteres Einsatzgebiet für Stammzellen dar. Es handelt sich dabei um eine multidisziplinäre Technologie, bei der Stammzellen sowie extrazelluläre Bestandteile (biologische und synthetische) verwendet werden, um im Labor „Gewebe“ zu entwickeln, die den PatientInnen wieder implantiert werden sollen.Tissue Engineering soll es einmal ermöglichen, komplexe Organe wie zum Beispiel die Leber außerhalb des menschlichen Körpers zu züchten, so die Vision. Dies erscheint schwierig, da dafür alle Zellen auch wirklich optimal mit Sauerstoff und Nahrung versorgt werden müssen und sich das gezüchtete Gewebe in den Organismus nahtlos einfügen muss.
Am besten erforscht ist derzeit die Herstellung von vitalem Hautersatz, der vor allem bei Personen mit großflächigen Verbrennungen benötigt wird. Darüber hinaus können bereits Knochen oder Knorpel gezüchtet werden, die in der Orthopädie bzw. der Zahn-, Kiefer und Knochenchirurgie zur Anwendung kommen. Auch „Minibrains“ können mittlerweile schon kultiviert werden. [5]
Anwendungen von Stammzellen: Ausblick und mögliche Gefahren
- ES-Zellen: Die klinische Anwendung von embryonalen Stammzellen ist in nächster Zukunft aus verschiedenen Gründen noch nicht absehbar. Da embryonale Stammzellen im Falle einer Transplantation höchstwahrscheinlich vom Immunsystem des Patienten/der Patientin als fremd erkannt und abgestoßen werden würden, gibt es den Ansatz des therapeutischen Klonens. Ziel dieser Technik ist es, embryonale Stammzellen herzustellen, die genetisch identisch mit dem Patienten/der Patientin sind und dadurch nicht vom Körper abgestoßen werden. Therapeutisches Klonen ist beim Menschen bis jetzt noch nicht gelungen. Abgesehen vom Problem der Abstoßung kann heute bei der Transplantation von Zellen, die aus embryonalen Stammzellen kultiviert wurden, eine Tumorbildung noch nicht ausgeschlossen werden: Befinden sich unter den transplantierten Zellen noch embryonale Stammzellen, die sich noch nicht in den gewünschten Zelltyp spezialisiert haben, können diese zu einem so genannten Teratom heranwachsen, einem Tumor aus unterschiedlichsten Zelltypen.
- iPS-Zellen: Für das Herstellen von iPS-Zellen gibt es mittlerweile mehrere Möglichkeiten, um Gene in Zellen einzuschleusen – ursprünglich wurden Retroviren als Vehikel verwendet. Da diese sich in die DNA integrieren, besteht dabei allerdings die Gefahr, dass sie mit wichtigen Genen interferieren und so Krebs auslösen könnten. Um iPS-Zellen zu validieren und zu verbessern, müsste eine große Anzahl dieser Zellen aus verschiedenen Individuen hergestellt und mit embryonalen Stammzellen verglichen werden. Eine patientInnen-spezifische Gewinnung erscheint unwahrscheinlich, da Stammzellen oft recht kurzfristig benötigt werden, wie beispielsweise nach einem Herzinfarkt. Vorstellbar ist eher eine Bank mit den verschiedensten iPS-Linien, die spezifische immunologische Eigenschaften besitzen, aus der dann eine immunologisch optimal geeignete gewählt wird. Allerdings müssen die Sicherheit und Eigenschaften von iPS-Zellen noch umfassend erforscht werden, bevor an einen Einsatz im Menschen überhaupt gedacht werden kann. Die Gefahr von genetischen Abnormitäten, Tumorbildung oder einer Abstoßung durch das Immunsystem kann zum aktuellen Zeitpunkt nicht ausgeschlossen werden.
as, 23.12.2019
Quellenangaben
[2] Tapan KG, Amit A., Mukta A. et al.: Current Status of Stem Cell Therapies in Tissue Repair and Regeneration (2019). Curr Stem Cell Res Ther, 14 (2), 117-126. DOI: 10.2174/1574888X13666180502103831
[3] Thomson JA, Itskovitz-Eldor J., Shapiro SS et al.: Embryonic Stem Cell Lines Derived From Human Blastocysts (1998). Science, , 282 (5391), 1145-7, 1998 Nov 6. DOI: 10.1126/science.282.5391.1145
[4] Takahashi K., Tanabe K., Ohnuki M. et al.: Induction of Pluripotent Stem Cells From Adult Human Fibroblasts by Defined Factors (2007). Cell, 131 (5), 861-72, 2007 Nov 30. DOI: 10.1016/j.cell.2007.11.019
[5] Lancaster MA, Renner M., Martin CM et al.: Cerebral organoids model human brain development and microcephaly (2013). Nature volume 501, pages373–379. DOI: 10.1038/nature12517